уран
- Історія
- Знаходження в природі
- ізотопи урану
- отримання
- Фізичні властивості
- Хімічні властивості
- застосування
- Геологія
- Інші СФЕРИ! Застосування
- збіднений уран
- Сердечники бронебійних снарядів
- Фізіологічна дія
- Розвідані запаси урану в світі
- Видобуток в Росії
- Видобуток в Казахстані
- Видобуток на Україні
- ВАРТІСТЬ
Уран Атомний номер 92 Зовнішній вигляд простої речовини  Властивості атома Атомна маса
Властивості атома Атомна маса
(Молярна маса) 238,0289 а. е. м. ( г / моль ) Радіус атома 138 пм енергія іонізації
(Перший електрон) 686,4 (7,11) кДж / моль ( еВ ) Електронна конфігурація [Rn] 5f3 6d1 7s2 Хімічні властивості Ковалентний радіус 142 пм радіус іона (+ 6e) 80 (+ 4e) 97 пм електронегативність
(По Полингу) 1,38 електродний потенціал U ← U4 + -1,38В
U ← U3 + -1,66В
U ← U2 + -0,1В ступені окислення 6, 5, 4, 3 Термодинамічні властивості щільність 19,05 г / см ³ Питома теплоємність 27,67 [1] Дж / ( K · моль ) теплопровідність 27,5 Вт / ( м · K ) Температура плавлення 1405,5 K теплота плавлення 12,6 кДж / моль Температура кипіння 4018 K теплота випаровування 417 кДж / моль молярний об'єм 12,5 см ³ / моль Кристалічна ґратка структура ґратки орторомбические параметри решітки 2,850 Å Ставлення c / a n / a температура Дебая n / a K U 92 238,0289 5f36d17s2 Уран
Уран (стара назва Ураній) - хімічний елемент з атомним номером 92 в періодичній системі, атомна маса 238,029; позначається символом U (Uranium), відноситься до сімейства актиноїдів.
Історія
Ще в найдавніші часи (I століття до нашої ери) природна окис урану використовувалася для виготовлення жовтої глазурі для кераміки. Дослідження урану розвивалися, подібно породжуваної їм ланцюгової реакції. Спочатку відомості про його властивості, як і перші імпульси ланцюгової реакції, надходили з великими перервами, від випадку до випадку. Перша важлива дата в історії урану - 1789 рік, коли німецький натурфілософ і хімік Мартін Генріх Клапрот відновив витягнуту з саксонської смоляний руди золотисто-жовту «землю» до чорного металлоподобного речовини. На честь самої далекої з відомих тоді планет (відкритої Гершелем вісьмома роками раніше) Клапрот, вважаючи нова речовина елементом, назвав його ураном.
П'ятдесят років уран Клапрота значився металом. Тільки в 1841 р Ежен Мелькіор Пелиго - французький хімік (1811-1890)] довів, що, незважаючи на характерний металевий блиск, уран Клапрота не елемент, а окисел UO2. У 1840 р Пелиго вдалося отримати справжній уран - важкий метал сіро-сталевого кольору і визначити його атомний вагу. Наступний важливий крок у вивченні урану зробив в 1874 р Д. І. Менделєєв. Спираючись на розроблену ним періодичну систему, він помістив уран в найдальшої клітці своєї таблиці. Перш атомний вага урану вважали рівним 120. Великий хімік подвоїв це значення. Через 12 років передбачення Менделєєва було підтверджено дослідами німецького хіміка Циммермана.
Вивчення урану почалося з 1896: французький хімік Антуан Анрі Беккерель випадково відкрив Промені Беккереля, які пізніше Марія Кюрі перейменувала в радіоактивність. В цей же час французькому хіміку Анрі Муассану вдалося розробити спосіб отримання чистого металевого урану. У 1899 р Резерфорд виявив, що випромінювання уранових препаратів неоднорідний, що є два види випромінювання - альфа і бета-промені. Вони несуть різний електричний заряд; далеко не однакові їх пробіг в речовині і іонізуюча здатність. Трохи пізніше, в травні 1900 р Поль Війар відкрив третій вид випромінювання - гамма-промені.
Ернест Резерфорд провів в 1907 р перші досліди з визначення віку мінералів при вивчення радіоактивних урану і торію на основі створеної ним спільно з Фредеріком Содді (Soddy, Frederick, 1877-1956; Нобелівська премія з хімії, 1921) теорії радіоактивності. У 1913 р Ф. Содді ввів поняття про ізотопи (від грец. Ισος - «рівний», «однаковий», і τόπος - «місце»), а в 1920 г.предсказал, що ізотопи можна використовувати для визначення геологічного віку гірських порід . У 1928 р Ніггот реалізував, а в 1939 р AOК.Нір (Nier, Alfred Otto Carl, 1911 - 1994) створив перші рівняння для розрахунку віку і застосував мас-спектрометр для розділення ізотопів.
У 1939 Фредерік Жоліо-Кюрі і німецькі фізики Отто Фріш і Ліза Мейтнер відкрили невідоме явище, що відбувається з ядром урану при опроміненні його нейтронами. Відбувалося вибуховий руйнування цього ядра з утворенням нових елементів набагато більш легких, ніж уран. Це руйнування носило вибухонебезпечне характер, оскільки продуктів розліталися в різні боки з величезними швидкостями. Таким чином було відкрито явище, назване ядерною реакцією.
У 1939-1940 рр. Ю. Б. Харитон і Я. Б. Зельдович вперше теоретично показали, що при невеликому збагаченні природного урану ураном-235 можна створити умови для безперервного поділу атомних ядер, тобто надати процесу ланцюговий характер.
Знаходження в природі
Уран широко поширений в природі. Кларк урану становить 1 · 10-3% (вага.). Кількість урану в шарі літосфери товщиною 20 км оцінюється в 1,3 · 1014 т.
Основна маса урану знаходиться в кислих породах з високим вмістом кремнію. Значна маса урану сконцентрована в осадових породах, особливо збагачених органікою. У великих кількостях як домішка уран присутній в торієвих і рідкоземельних мінералів (ортит, Стено CaTiO3 [SiO4], монацит (La, Ce} PO4, циркон ZrSiO4, ксенотим YPO4 і ін.). Найважливішими уранові руди є настуран (уранова смілка), уранініт і карнотіт. Основними мінералами - супутниками урану є молибденит MoS2, галеніт PbS, кварц SiO2, кальцит CaCO3, гидромуськовіт і ін.
Мінерал Основний склад мінералу Вміст урану,% Уранініт UO2, UO3 + ThO2, CeO2 65-74 карнотіт K2 (UO2) 2 (VO4) 2 · 2H2O ~ 50 Казоле PbO2 · UO3 · SiO2 · H2O ~ 40 Самарська (Y, Er, Ce , U, Ca, Fe, Pb, Th) · (Nb, Ta, Ti, Sn) 2O6 3.15-14 Браннер (U, Ca, Fe, Y, Th) 3Ti5O15 40 тюямуніт CaO · 2UO3 · V2O5 · nH2O 50-60 Цейнера Cu (UO2) 2 (AsO4) 2 · nH2O 50-53 Отенія Ca (UO2) 2 (PO4) 2 · nH2O ~ 50 Шрекінгеріт Ca3NaUO2 (CO3) 3SO4 (OH) · 9H2O 25 Уранофан CaO · UO2 · 2SiO2 * 6H2O ~ 57 Фергюсон (Y, Ce) (Fe, U) (Nb, Ta) O4 0.2-8 Торберн Cu (UO2) 2 (PO4) 2 · nH2O ~ 50 Коффіна U (SiO4) 1-x (OH) 4x ~ 50
Основними формами знаходжень урану в природі є уранініт, настуран (уранова смілка) і уранові черні. Вони відрізняються тільки формами знаходження; є вікова залежність: уранініт присутній переважно в древніх (докембрійських породах), настуран - вулканогенний і гідротермальний - переважно в палеозойських і більш молодих високо- і среднетемпературних утвореннях; уранові черні - в основному в молодих - кайнозойських і молодше утвореннях - переважно в низькотемпературних осадових породах.
Вміст урану в земній корі становить 0,003%, він зустрічається в поверхневому шарі землі у вигляді чотирьох видів відкладень. По-перше, це жили уранініта, або уранової смолки (діоксид урану UO2), дуже багаті ураном, але рідко зустрічаються. Їм супроводжують відкладення радію, так як радій є прямим продуктом ізотопного розпаду урану. Такі жили зустрічаються в Заїрі, Канаді (Велике Ведмеже озеро), Чехії та Франції. Ще одне джерело урану є конгломерати ториевой і уранової руди спільно з рудами інших важливих мінералів. Конгломерати зазвичай містять достатні для отримання кількості золота і срібла, а супутніми елементами стають уран і торій. Великі родовища цих руд знаходяться в Канаді, ПАР, Росії та Австралії. Третім джерелом урану є осадові породи і пісковики, багаті мінералом карнотиту (ураніл-ванадат калію), який містить, окрім урану, значна кількість ванадію та інших елементів. Такі руди зустрічаються в західних штатах США. Железоурановие сланці і фосфатні руди становлять четвертий джерело відкладень. Багаті відкладення виявлені в глинистих сланцях Швеції. Деякі фосфатні руди Марокко і США містять значні кількості урану, а фосфатні поклади в Анголі і Центральноафриканській Республіці ще більш багаті ураном. Більшість лігнітів і деякі вугілля зазвичай містять домішки урану. Багаті ураном відкладення лігнітів виявлені в Північній і Південній Дакоті (США) і бітумних вугіллі Іспанії та Чехії
ізотопи урану
Природний уран складається з суміші трьох ізотопів: 238U - 99,2739% (період напіврозпаду T 1/2 = 4,468 × 109 років), 235U - 0,7024% (T 1/2 = 7,038 × 108 років) і 234U - 0, 0057% (T 1/2 = 2,455 × 105 років). Останній ізотоп є не первинним, а радіогенним, він входить до складу радіоактивного ряду 238U.
Радіоактивність природного урану обумовлена в основному ізотопами 238U і 234U, в рівновазі їх питомі активності рівні. Питома активність ізотопу 235U в природному урані в 21 разів менше активності 238U.
Відомо 11 штучних радіоактивних ізотопів урану з масовими числами від 227 до 240. Найбільш довгоживучий з них - 233U (T 1/2 = 1,62 × 105лет) виходить при опроміненні торію нейтронами і здатний до спонтанного поділу тепловими нейтронами.
Ізотопи урану 238U і 235U є родоначальниками двох радіоактивних рядів. Кінцевими елементами цих рядів є ізотопи свинцю 206Pb і 207Pb.
У природних умовах поширені в основному ізотопи 234U: 235U: 238U = 0,0054: 0,711: 99,283. Половина радіоактивності природного урану обумовлена ізотопом 234U. Ізотоп 234U утворюється за рахунок розпаду 238U. Для двох останніх на відміну від інших пар ізотопів і незалежно від високої міграційної здатності урану характерно географічне сталість відносини 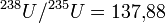 . Величина цього відношення залежить про віку урану. Численні натурні вимірювання показали його незначні коливання. Так в ролах величина цього відношення щодо еталона змінюється в межах 0,9959 -1,0042, в солях - 0,996 - 1,005. У урансодержащих мінералах (настуран, уранова чернь, ціртоліт, рідкоземельні руди) величина цього відношення коливається в межах 137,30 - 138,51; причому відмінність між формами UIV і UVI не встановлено; в сфена - 138,4. В окремих метеоритах виявлено нестачу ізотопу 235U. Найменша його концентрація в земних умовах знайдена в 1972 р французьким дослідником Бужігесом в містечку Окло в Африці (родовище в Габоні). Так в нормальному урані міститься 0,7025% урану 235U, тоді як в Окло воно зменшуються до 0,557%. Це послужило підтвердженням гіпотези про наявність природного ядерного реактора, що веде до вигоряння ізотопу, передбаченої Джордж Ветрілл (George W. Wetherill) з Каліфорнійського університету в ЛосАнджелесе і Марк Інгремом (Mark G. Inghram) із Чиказького університету і Полом Курода (Paul K. Kuroda) , хіміком з Університету Арканзасу, ще в 1956 р описав процес. Крім цього, в цих же округах знайдені природні ядерні реактори: Окелобондо, Бангомбе (Bangombe) і ін. В даний час відомо близько 17 природних ядерних реакторів.
. Величина цього відношення залежить про віку урану. Численні натурні вимірювання показали його незначні коливання. Так в ролах величина цього відношення щодо еталона змінюється в межах 0,9959 -1,0042, в солях - 0,996 - 1,005. У урансодержащих мінералах (настуран, уранова чернь, ціртоліт, рідкоземельні руди) величина цього відношення коливається в межах 137,30 - 138,51; причому відмінність між формами UIV і UVI не встановлено; в сфена - 138,4. В окремих метеоритах виявлено нестачу ізотопу 235U. Найменша його концентрація в земних умовах знайдена в 1972 р французьким дослідником Бужігесом в містечку Окло в Африці (родовище в Габоні). Так в нормальному урані міститься 0,7025% урану 235U, тоді як в Окло воно зменшуються до 0,557%. Це послужило підтвердженням гіпотези про наявність природного ядерного реактора, що веде до вигоряння ізотопу, передбаченої Джордж Ветрілл (George W. Wetherill) з Каліфорнійського університету в ЛосАнджелесе і Марк Інгремом (Mark G. Inghram) із Чиказького університету і Полом Курода (Paul K. Kuroda) , хіміком з Університету Арканзасу, ще в 1956 р описав процес. Крім цього, в цих же округах знайдені природні ядерні реактори: Окелобондо, Бангомбе (Bangombe) і ін. В даний час відомо близько 17 природних ядерних реакторів.
отримання
Найперша стадія уранового виробництва - концентрування. Породу подрібнюють і змішують з водою. Важкі компоненти суспензії осідають швидше. Якщо порода містить первинні мінерали урану, то вони осідають швидко: це важкі мінерали. Вторинні мінерали урану легше, в цьому випадку раніше осідає важка порожня порода. (Втім, далеко не завжди вона дійсно порожня, в ній можуть бути багато корисні елементи, в тому числі і уран).
Наступна стадія - вилуговування концентратів, переклад урану в розчин. Застосовують кислотне і лужне вилуговування. Перше - дешевше, оскільки для вилучення урану використовують сірчану кислоту. Але якщо у вихідній сировині, як, наприклад, в урановій смолці, уран знаходиться в чотиривалентність стані, то цей спосіб непридатний: чотиривалентність уран в сірчаної кислоти практично не розчиняється. В цьому випадку потрібно або вдатися до лужного вилуговування, або попередньо окисляти уран до шестивалентного стану.
Чи не застосовують кислотне вилуговування і в тих випадках, якщо урановий концентрат містить доломіт або магнезит, що реагують з сірчаною кислотою. У цих випадках користуються їдким натром (гідроксидом натрію).
Проблему вилуговування урану з руд вирішує киснева продування. У нагріту до 150 ° C суміш уранової руди з сульфідними мінералами подають потік кисню. При цьому з сірчистих мінералів утворюється сірчана кислота, яка і вимиває уран.
На наступному етапі з отриманого розчину потрібно вибірково виділити уран. Сучасні методи - екстракція і іонний обмін - дозволяють вирішити цю проблему.
Розчин містить не тільки уран, але і інші катіони. Деякі з них в певних умовах поводяться так само, як уран: екстрагуються тими ж органічними розчинниками, осідають на тих же іонообмінних смолах, випадають в осад при тих же умовах. Тому для селективного виділення урану доводиться використовувати багато окислювально-відновні реакції, щоб на кожній стадії позбавлятися від того чи іншого небажаного попутника. На сучасних іонообмінних смолах уран виділяється досить селективно.
Методи іонного обміну і екстракції гарні ще й тим, що дозволяють досить повно витягувати уран з бідних розчинів (вміст урану - десяті частки грама на літр).
Після цих операцій уран переводять в твердий стан - в один з оксидів або в тетрафторид UF4. Але цей уран ще треба очистити від домішок з великим перетином захоплення теплових нейтронів - бору, кадмію, гафнію. Їх зміст в кінцевому продукті не повинно перевищувати стотисячних і мільйонних часток відсотка. Для видалення цих домішок технічно чисте з'єднання урану розчиняють в азотній кислоті. При цьому утворюється уранілнітрату UO2 (NO3) 2, який при екстракції трибуто-фосфатом і деякими іншими речовинами додатково очищається до потрібних кондицій. Потім ця речовина кристалізують (або осаджують пероксид UO4 · 2H2O) і починають обережно прожарювати. В результаті цієї операції утворюється трехокісь урану UO3, яку відновлюють воднем до UO2.
На діоксид урану UO2 при температурі від 430 до 600 ° C впливають сухим фтористим воднем для отримання тетрафторида UF4. З цього з'єднання відновлюють металевий уран за допомогою кальцію або магнію.
Фізичні властивості
Уран - дуже важкий, сріблясто-білий глянцюватий метал. У чистому вигляді він трохи м'якше стали, ковкий, гнучкий, володіє невеликими парамагнітні властивості. Уран має три аллотропние форми: альфа (призматична, стабільна до 667,7 ° C), бета (чотирикутна, стабільна від 667,7 ° C до 774,8 ° C), гамма (з об'ємно центрованої кубічної структурою, що існує від 774, 8 ° C до точки плавлення).
Радіоактивні властивості деяких ізотопів урану (виділені природні ізотопи):
Масове число Період напіврозпаду Тип розпаду 234 2,45 · 105 років α 235 7,13 · 108 років α 236 2,39 · 107 років α 237 6,75 сут. β- 238 4,49 · 109 років α 239 23,54 хв. β- 240 14 годину. β-
Хімічні властивості
Уран може проявляти ступеня окислення від + III до + VI. Сполуки урану (III) утворюють нестійкі розчини червоного кольору і є сильними відновниками:
4UCl3 + 2H2O → 3UCl4 + UO2 + H2 ↑
Сполуки урану (IV) є найбільш стійкими і утворюють водні розчини зеленого кольору.
Сполуки урану (V) нестійкі і легко диспропорционируют у водному розчині:
2UO2Cl → UO2Cl2 + UO2
Хімічно уран дуже активний метал. Швидко окислюючись на повітрі, він покривається райдужною плівкою оксиду. Дрібний порошок урану самозаймається на повітрі, він запалюється при температурі 150-175 ° C, утворюючи U3O8. При 1000 ° C уран з'єднується з азотом, утворюючи жовтий нітрид урану. Вода здатна роз'їдати метал, повільно при низькій температурі, і швидко при високій, а також при дрібному подрібненні порошку урану. Уран розчиняється в соляній, азотній і інших кислотах, утворюючи чотиривалентність солі, зате не взаємодіє з лугами. Уран витісняє водень з неорганічних кислот і сольових розчинів таких металів, як ртуть, срібло, мідь, олово, платина і золото. При сильному струшуванні металеві частинки урану починають світитися. Уран має чотири ступені окислення - III-VI. Шестивалентного сполуки включають в себе триокис урану (окис уранила) UO3 і уранілхлорід урану UO2Cl2. Тетрахлорид урану UCl4 і діоксид урану UO2 - приклади четирехвалентного урану. Речовини, що містять чотиривалентність уран, зазвичай нестабільні і звертаються в шестивалентний при тривалому перебуванні на повітрі. Ураніловие солі, такі як уранілхлорід, розпадаються в присутності яскравого світла або органіки.
застосування
ядерне паливо
Найбільше застосування має ізотоп урану 235U, в якому можлива самопідтримується ланцюгова ядерна реакція. Тому цей ізотоп використовується як паливо в ядерних реакторах, а також в ядерній зброї. Виділення ізотопу U235 з природного урану - складна технологічна проблема, (див. Поділ ізотопів).
Ізотоп U238 здатний ділитися під впливом бомбардування високоенергетичними нейтронами, цю його особливість використовують для збільшення потужності термоядерного зброї (використовуються нейтрони, породжені термоядерної реакцією).
В результаті захоплення нейтрона з подальшим β-розпадом 238U може перетворюватися в 239Pu, який потім використовується як ядерне паливо.
Уран-233, штучно одержуваний в реакторах з торія (торій-232 захоплює нейтрон і перетворюється в торій-233, який розпадається в протактиний-233 і потім в уран-233), може в майбутньому стати поширеним ядерним паливом для атомних електростанцій (вже зараз існують реактори, що використовують цей нуклід в якості палива, наприклад KAMINI в Індії) і виробництва атомних бомб (критична маса близько 16 кг).
Уран-233 також є найбільш перспективним паливом для газофазних ядерних ракетних двигунів.
Геологія
Основна галузь використання урану - визначення віку мінералів і гірських порід з метою з'ясування послідовності протікання геологічних процесів. Цим займаються Геохронологія та Теоретична геохронология. Суттєве значення має також рішення задачі про змішування і джерелах речовини.
В основі рішення задачі лежать рівняння радіоактивного розпаду, описуваних рівняннями.
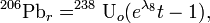
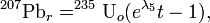
де 238Uo, 235Uo - сучасні концентрації ізотопів урану; 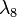 ;
; 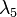 - постійні розпаду атомів відповідно урану 238U і 235U.
- постійні розпаду атомів відповідно урану 238U і 235U.
Дуже важливим є їх комбінація:
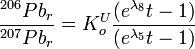
.
тут
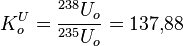
У зв'язку с тім, что гірські породи містять Різні концентрації урану, смороду ма ють різну радіоактівністю. Ця властівість вікорістовується при віділенні гірськіх порід геофізичними методами. Найбільш широко цей метод застосовується в нафтовій геології при геофізичних дослідженнях свердловин, в цей комплекс входить, зокрема, γ - каротаж або нейтронний гамма-каротаж, гамма-гамма-каротаж і т. Д. З їх допомогою проісходт виділення колекторів і флюідоупорамі.
Інші СФЕРИ! Застосування
Невелика добавка урану надає гарну жовто-зелену флуоресценцію склу (Уранове скло).
Уранати натрію Na2U2O7 використовувався як жовтий пігмент в живопису.
Сполуки урану застосовувалися як фарби для живопису по фарфору і для керамічної глазурі і емалей (фарбують в кольори: жовтий, бурий, зелений і чорний, в залежності від ступеня окислення).
Деякі сполуки урану світлочутливі.
На початку XX століття уранілнітрату широко застосовувався для посилення негативів і фарбування (тонування) позитивів (фотографічних відбитків) в бурий колір.
Карбід урану-235 в сплаві з карбідом ніобію і карбідом цирконію застосовується в якості палива для ядерних реактивних двигунів (робоче тіло - водень + гексан).
Сплави заліза і збідненого урану (уран-238) застосовуються як потужні магнітострикційні матеріали.
збіднений уран
збіднений уран
Вийнявши 235U і 234U з природного урану, решту матеріалу (уран-238) носить назву «збіднений уран», так як він збіднений 235-м ізотопом. За деякими даними, в США зберігається близько 560 000 тон збідненого гексафториду урану (UF6).
Збіднений уран в два рази менш радіоактивний, ніж природний уран, в основному за рахунок видалення з нього 234U. Через те, що основне використання урану - виробництво енергії, збіднений уран - малокорисних продукт з низькою економічної цінності.
В основному його використання пов'язане з великою щільністю урану і відносно низькою його вартістю. Збіднений уран використовується для радіаційного захисту (як це не дивно) і як баластних маса в аерокосмічних застосуваннях, таких як рульові поверхні літальних апаратів. У кожному літаку «Боїнг-747» міститься 1500 кг збідненого урану для цих цілей. Ще цей матеріал застосовується в високошвидкісних роторах гіроскопів, великих маховиках, як баласт в космічних апаратах, що спускаються і гоночних яхтах, при бурінні нафтових свердловин.
Сердечники бронебійних снарядів
Найвідоміше застосування збідненого урану - як осердя для бронебійних снарядів. При сплаві з 2% Mo або 0,75% Ti і термічній обробці (швидка гарт розігрітого до 850 ° C металу у воді або маслі, подальше витримування при 450 ° C 5 годин) металевий уран стає твердіше і міцніше сталі (міцність на розрив більше 1600 МПа, при тому, що у чистого урану вона дорівнює 450 МПа). У поєднанні з великою щільністю, це робить загартовану уранову болванку надзвичайно ефективним засобом для пробивання броні, аналогічним по ефективності більш дорогому вольфраму. Важкий урановий наконечник також змінює розподіл мас в снаряді, покращуючи його аеродинамічну стійкість.
Подібні сплави типу «Стабілла» застосовуються в стреловидних оперених снарядах танкових і протитанкових артилерійських знарядь.
Процес руйнування броні супроводжується подрібненням в пил уранової болванки і займанням її на повітрі з іншого боку броні (див. Пірофорному). Близько 300 тонн збідненого урану залишилися на полі бою під час операції «Буря в пустелі» (здебільшого це залишки снарядів 30-мм гармати GAU-8 штурмових літаків A-10, кожен снаряд містить 272 г уранового сплаву).
Такі снаряди були використані військами НАТО в бойових діях на території Югославії. Після їх застосування обговорювалася екологічна проблема радіаційного забруднення території країни.
Вперше уран в якості сердечника для снарядів був застосований в Третьому рейху.
Збіднений уран використовується в сучасній танкової броні, наприклад, танка M-1 «Абрамс».
Фізіологічна дія
У микроколичествах (10-5-10-8%) виявляється в тканинах рослин, тварин і людини. Найбільшою мірою накопичується деякими грибами і водоростями. Сполуки урану всмоктуються в шлунково-кишковому тракті (близько 1%), в легенях - 50%. Основні депо в організмі: селезінка, нирки, скелет, печінку, легені і бронхо-легеневі лімфатичні вузли. Зміст в органах і тканинах людини і тварин не перевищує 10-7г.
Уран і його сполуки токсичні. Особливо небезпечні аерозолі урану і його сполук. Для аерозолів розчинних у воді сполук урану ПДК в повітрі 0,015 мг / м³, для нерозчинних форм урану ПДК 0,075 мг / м³. При попаданні в організм уран діє на всі органи, будучи загальноклітинними отрутою. Молекулярний механізм дії урану пов'язаний з його здатністю пригнічувати активність ферментів. В першу чергу уражаються нирки (з'являються білок і цукор в сечі, олігурія). При хронічній інтоксикації можливі порушення кровотворення і нервової системи.
Розвідані запаси урану в світі
Видобуток урану в світі
Згідно з «Червоною книгою по урану», випущеної ОЕСР, в 2005 видобуто 41 250 тонн урану (в 2003 - 35 492 тонни). Згідно з даними ОЕСР, в світі функціонує 440 реакторів комерційного призначення, які споживають на рік 67 тис. Тонн урану. Це означає, що його виробництво забезпечує лише 60% обсягу його споживання (інше витягується зі старих ядерних боєголовок).
Видобуток по країнах в тоннах за змістом U на 2005-2006 рр.
Країна 2005 рік Канада 11 410 Австралія 9044 Казахстан 4020 Росія 3570 США 1249 Україна 920 Китай 920
Видобуток по компаніях в 2006 р .:
Cameco - 8,1 тис. Тонн
Rio Tinto - 7 тис. Тонн
AREVA - 5 тис. Тонн
Казатомпром - 3,8 тис.тонн
ВАТ ТВЕЛ - 3,5 тис. Тонн
BHP Billiton - 3 тис. Тонн
Навоийский ГМК - 2,1 тис. Тонн (Узбекистан, Навої)
Uranium One - 1 тис. Тонн
Heathgate - 0,8 тис. Тонн
Denison Mines - 0,5 тис. Тонн
Видобуток в Росії
В СРСР основними ураноруднимі регіонами були Україна (родовище Жовторіченського, Первомайське та ін.), Казахстан (Північний - Балкашінское рудне поле та ін .; Південний - Кизилсайское рудне поле та ін .; Східний; всі вони належать переважно вулканогенно -гідротермальному типу); Забайкаллі (Антей, Стрілецький і ін.); Середня Азія, в основному Узбекистан з зруденінням в чорних сланцях з центром в м Учкудук. Є маса дрібних рудопроявлений і проявів. У Росії основним урановорудним регіоном залишилося Забайкаллі. На родовищі в Читинській області (біля міста Краснокаменськ) видобувається близько 93% російського урану. Видобуток здійснює шахтним способом «Приаргунск виробниче гірничо-хімічне об'єднання» (ППГХО), що входить до складу ВАТ «Атомредметзолото» (урановий холдинг).
Решта 7% отримують методом підземного вилуговування ЗАТ «Далур» (Курганська область) і ВАТ «Хіагда» (Бурятія).
Отримані руди і урановий концентрат переробляються на Чепецькому механічному заводі.
Видобуток в Казахстані
У Казахстані зосереджена приблизно п'ята частина світових запасів урану (21% і 2 місце в світі). Загальні ресурси урану близько 1,5 млн. Тонн, з них близько 1,1 млн. Тонн можна видобувати методом підземного вилуговування.
У 2009 році Казахстан вийшов на перше місце в світі з видобутку урану.
Видобуток на Україні
Основне підприємство - Східний гірничо-збагачувальний комбінат в місті Жовті Води.
ВАРТІСТЬ
Незважаючи на існуючі легенди про десятки тисяч доларів за кілограмові або навіть грамові кількості урану, реальна його ціна на ринку не дуже висока - незбагаченого окис урану U3O8 дешевше 100 американських доларів за кілограм. Пов'язано це з тим, що для запуску атомного реактора на незбагаченого урані потрібні десятки або навіть сотні тонн палива, а для виготовлення ядерної зброї слід збагатити велику кількість урану для отримання придатних для створення бомби концентрацій